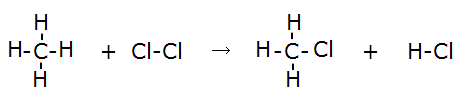Confira questões resolvidas sobre a Energia de Ligação:
1) (UniCESUMAR-SP) – A ligação covalente que mantém os átomos de nitrogênio e oxigênio unidos no óxido nítrico, NO, não é explicada pela regra do octeto, mas a sua energia de ligação pode ser calculada a partir dos dados fornecidos abaixo. Dados:
Energia de ligação N≡N: 950 kJ.mol–1;
Energia de ligação O=O: 500 kJ.mol–1;
Entalpia de formação do NO: 90 kJ.mol–1.
A partir dessas informações, é possível concluir que a energia de ligação entre os átomos de nitrogênio e oxigênio no óxido nítrico é:
N2 + O2 → 2NO
a) 90 kJ.mol–1.
b) 680 kJ.mol–1.
c) 765 kJ.mol–1.
d) 1360 kJ.mol–1.
e) 1530 kJ.mol–1.
3) UFRGS 2015 – A reação de cloração do metano, em presença de luz, é mostrada abaixo.
CH4 + Cl2 → CH3Cl + HCl ΔH = -25 kcal.mol-1
Considere os dados de energia das ligações abaixo.
C-H = 105 kcal.mol-1
Cl-Cl = 58 kcal.mol-1
H-Cl = 103 kcal.mol-1
A energia da ligação C-Cl, no composto CH3Cl, é
(A) 33 kcal.mol-1 .
(B) 56 kcal.mol-1 .
(C) 60 kcal.mol-1 .
(D) 80 kcal.mol-1 .
(E) 85 kcal.mol-1
4HCl(g) + O2(g) → 2H2O(g) + 2Cl2(g) é:
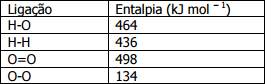
Dados: (Energia de ligação em kcal/mol)
H–Cl: 103,1; H–O: 110,6; O=O: 119,1; Cl–Cl: 57,9.
a) + 1089,2 kcal
b) – 467,4 kcal
c) -26,7 kcal
d) +911,8 kcal