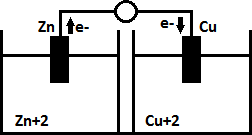
Confira questões resolvidas sobre as Pilhas:
a) Zn+ + e- → Zn
b) Zn2+ + 2e- → Zn
c) Zn → Zn+ + e-
d) Zn → Zn2+ + 2e-
e) Zn2+ + Zn → 2Zn+
3) (Enem cancelado 2009) – Pilhas e baterias são dispositivos tão comuns em nossa sociedade que, sem percebermos, carregamos vários deles junto ao nosso corpo; elas estão presentes em aparelhos de MP3, relógios, rádios, celulares etc. As semirreações descritas a seguir ilustram o que ocorre em uma pilha de óxido de prata. Pode-se afirmar que esta pilha
a) é uma pilha ácida.
b) apresenta o óxido de prata como o ânodo.
c) apresenta o zinco como o agente oxidante.
d) tem como reação da célula a seguinte reação: Zn(s) + Ag2O(s) → ZnO(s) + 2Ag(s)
e) apresenta fluxo de elétrons na pilha do eletrodo de Ag2O para o Zn.
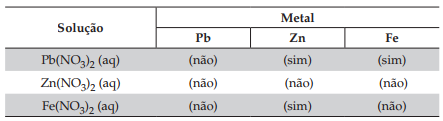
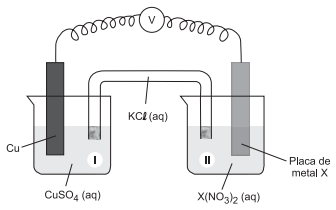
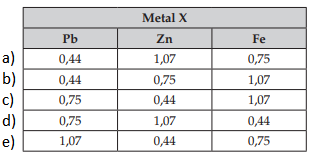
4) (PUC-MG) – Considere a célula eletroquímica, representada pela equação global:
Ni + Cu2+ → Ni2+ + Cu
É correto afirmar que:
a) há desgaste do eletrodo de cobre.
b) o cobre sofre oxidação.
c) o níquel funciona como ânodo.
d) a solução de níquel dilui-se.
e) os elétrons fluem, pelo circuito externo, do cobre para o níquel.
positivo) ocorrem reações de redução.
Na e Cl2 (g).
oxidação e no ânodo reações de oxidação.
é do ânodo para o cátodo.

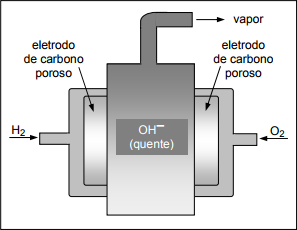
para o ensino médio. Vol. único. São Paulo: Scipione,
2002, p. 307.
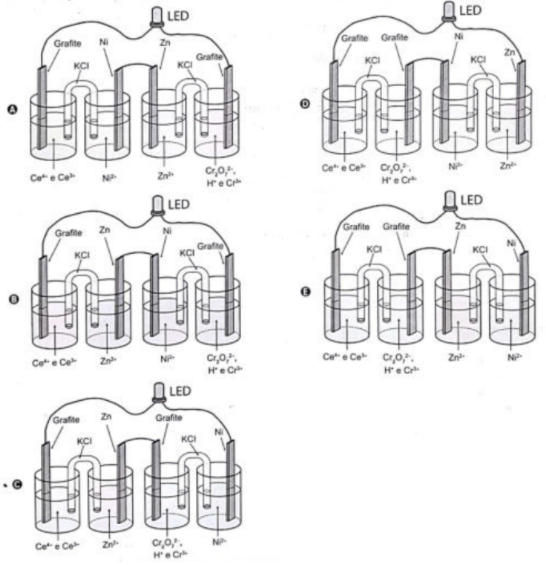
da figura acima, assinale a(s) proposição(ões)
CORRETA(S).
oxidante.
pilha é + 1,23 V.
dispositivo é um processo espontâneo.
padrão é 2 H2 (g) + O2 (g) → 2 H2O(l).
pilha é + 0,43 V.